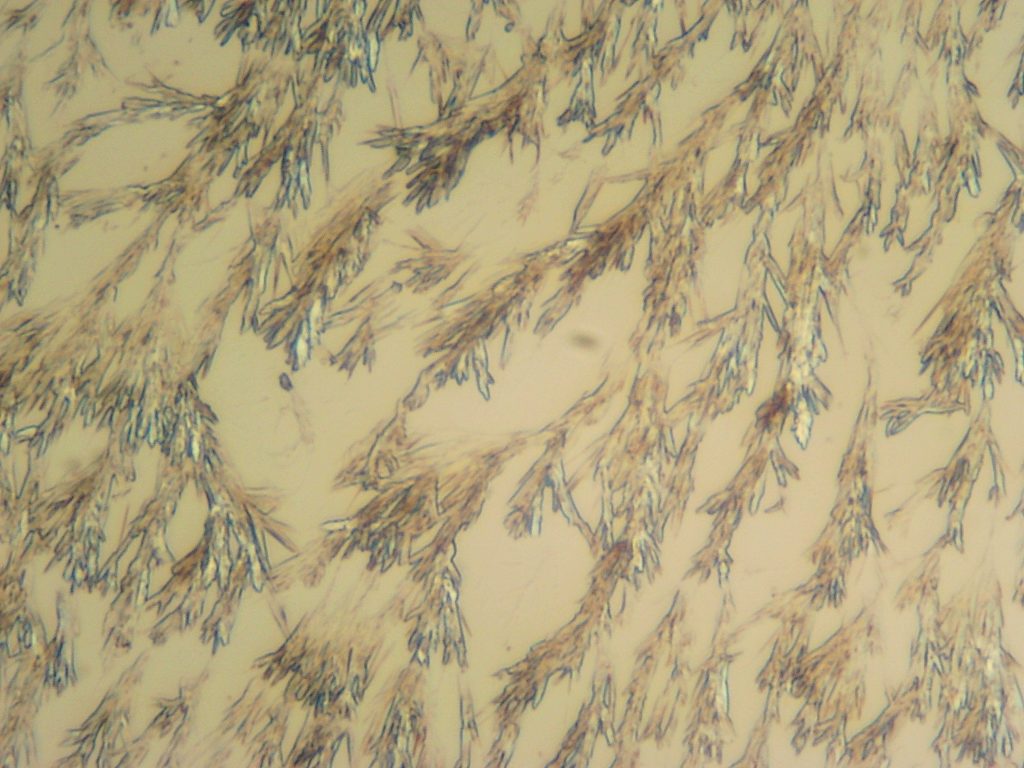
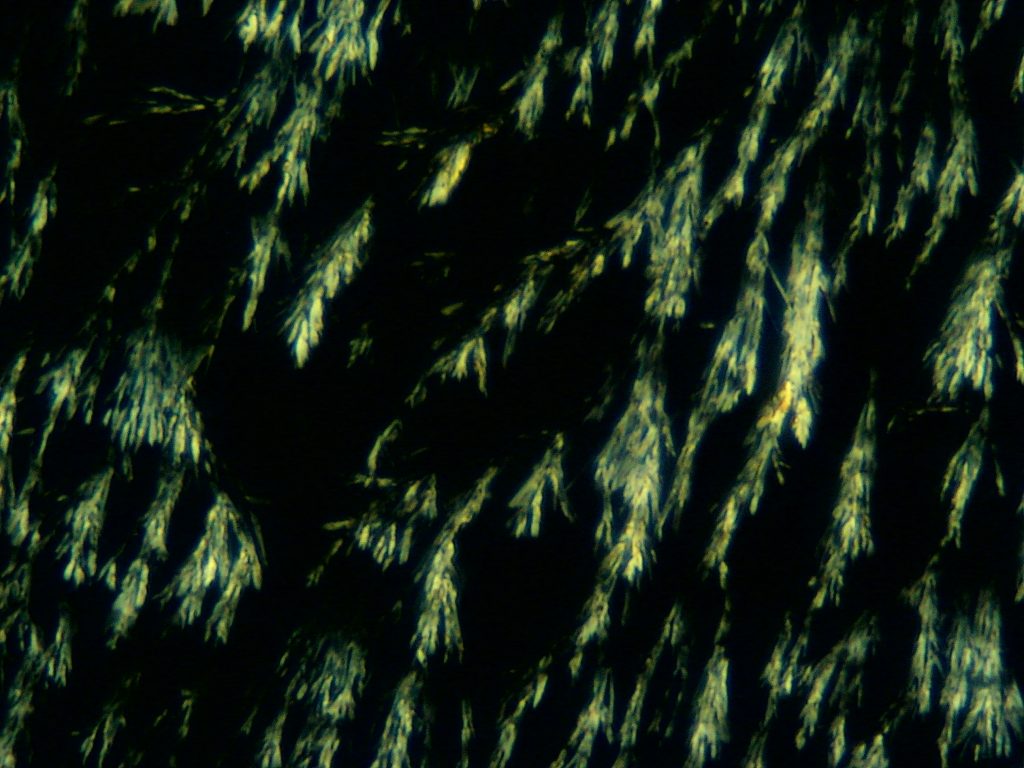
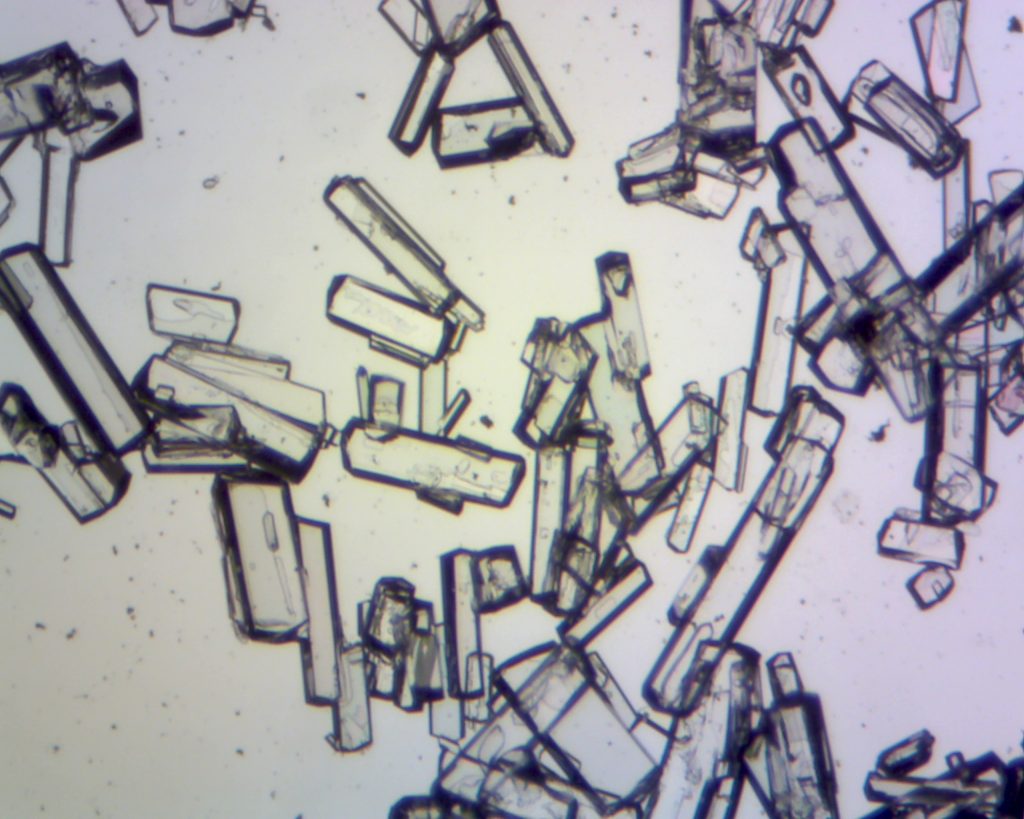
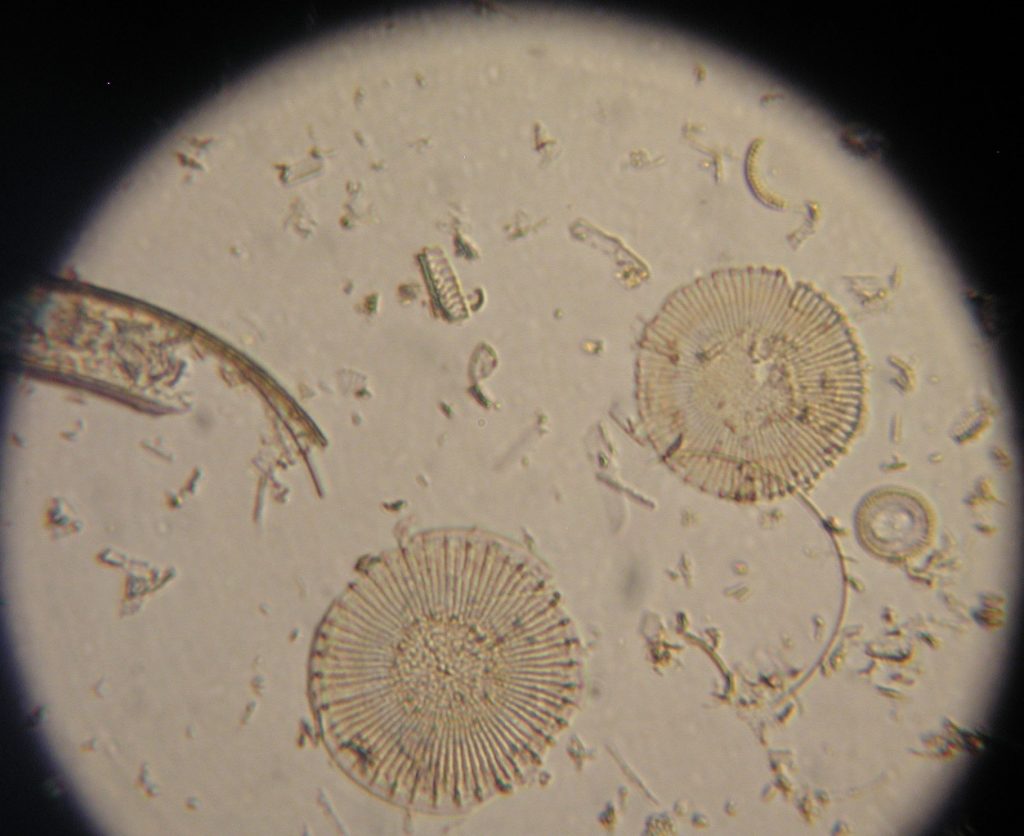
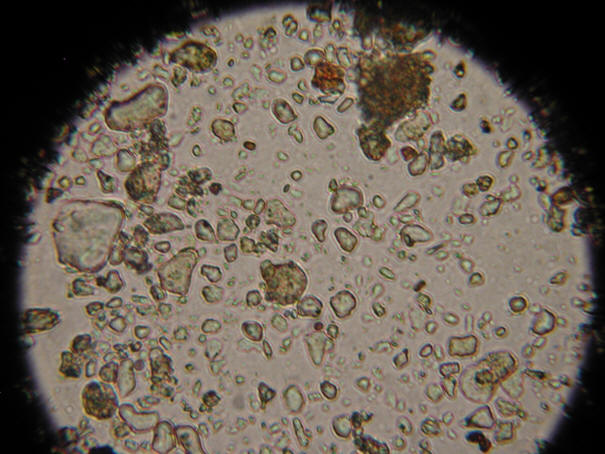
Microkristallen onder de microscoop maar vooral onder de polarisatiemicroscoop te bekijken is een avontuur. Soms kan het echter een probleem zijn stoffen in de juiste zuiverheid te vinden. Goed rondkijken bij de drogist kan dan echter zeer behulpzaam zijn. Daar kan men bv wrattentinctuur vinden, een oplossing van salicylzuur (ortho-hydroxy-benzoezuur, 170 mg/ml). Doe een druppeltje van deze oplossing op een objectglaasje waar al een druppel water op ligt, meng goed, damp voorzichtig in op een verwarmingsplaatjes (b.v. USB warmhoudplaat) en bekijk het preparaat onder de microscoop. Men kan dan naaldvormige kristallen waarnemen die onder gepolariseerd licht verschillend kleuren laten zien. Het oplosmiddel van Formule W is vermoedelijk niet alleen maar water. Bij het maken van preparaten vindt nogal gemakkelijk gelering plaats. De bijsluiter vermeldt als andere bestanddelen (hulpstoffen) aceton, alcohol, ricinusolie (wonderolie) en nitrocellulose. Vermoedelijk is de nitrocellulose verantwoordelijk voor de gelering. Het kan daarom zijn dat men het enkele malen moet proberen alvorens men een goed preparaat heeft. Men kan ook verschillende verdunningsmiddelen uitproberen waarbij ik zelf aan de slag ben gegaan met demi water, bioethanol, isopropanol, water/glycerine en aceton. Bij gebruik van aceton heeft men het minste last van gelering, hetgeen men ook mag verwachten op basis van de formulering.
Na het experiment ben ik nog in enkel boeken gaan neuzen om te kijken of ik nog recepten kon vinden voor wrattentinctuur. Edel geeft in “Mengen en Roeren Deel 1” (9de druk) de volgende formuleringen op als wrattenmiddel:
I: 2 dl salicylzuur en 20 dl ijsazijn
II: 90 dl trichloorazijnzuur en 10 dl water